
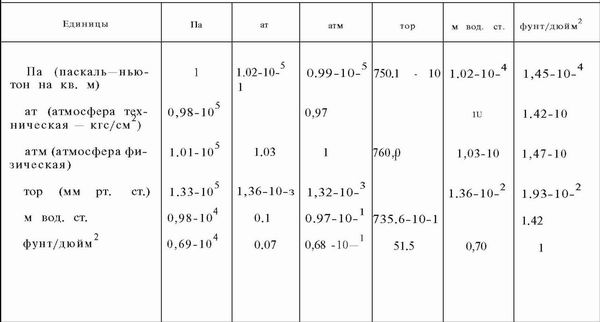
Зависимость давления газа от объема и температуры
Ее называют постоянной Больцмана , в честь австрийского физика Л. Больцмана, одного из создателей молекулярно-кинетической теории. Постоянная Больцмана — одна из фундаментальных физических констант. Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул.



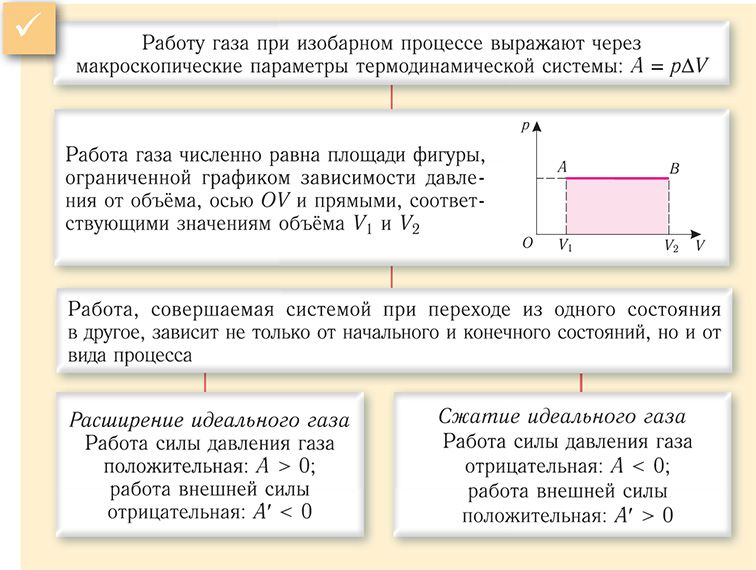

![Уравнение состояния идеального газа [ М Г Т У ]](https://cdn-user84060.skyeng.ru/uploads/60530c9c86266386805380.png)

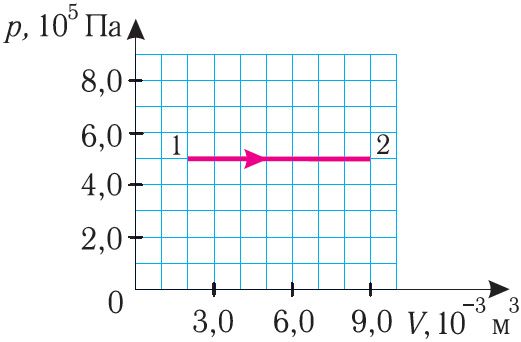
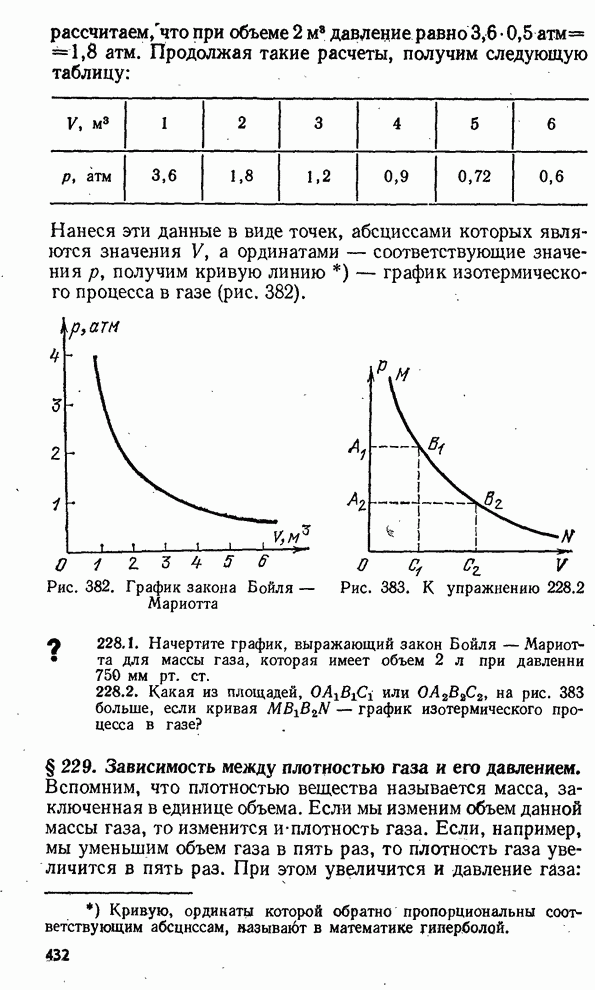
Описывает поведение газа в изотермическом процессе. С точки зрения современной физики закон представляет собой следствие Уравнения состояния идеального газа [2]. Утверждение закона Бойля — Мариотта состоит в следующем [3] [4] [5] :. При постоянных температуре и массе газа произведение давления газа на его объём постоянно.
- Идеальный газ
- Перевод статьи с англоязычной вики. В этой статье пойдёт речь о физике процессов связанной с давлением, объемом, количеством и температурой газа.
- Уравнение состояния термодинамической системы представляет собой аналитическую формулу, связывающую параметры состояния системы.
- Письмо с инструкцией по восстановлению пароля будет отправлено на вашу почту. Известно, что все вещества состоят из молекул, между которыми есть расстояния.
- Расчет объема идеального газа
- Вход Регистрация. Учебные заведения.
- Просто ЕГЭ. Какие формулы и законы необходимо знать для успешной сдачи раздела молекулярной физики в ЕГЭ?
- Без газа наш мир выглядел бы иначе: никто бы не мог дышать, атмосферы бы не существовало, смешных голосов из-за гелия бы не получалось.
- Зависимость давления от других величин
- Организатор олимпиад, репетитор по физике, математике и информатике, программист. Автор 17 публикаций в научных изданиях.
- Вход Регистрация. Учебные заведения.
- Идеальный газ — это основное понятие в физике и химии, которое помогает нам понять, как вещества взаимодействуют друг с другом при различных условиях.


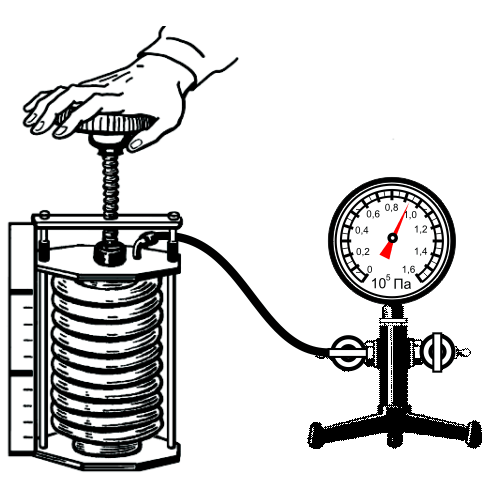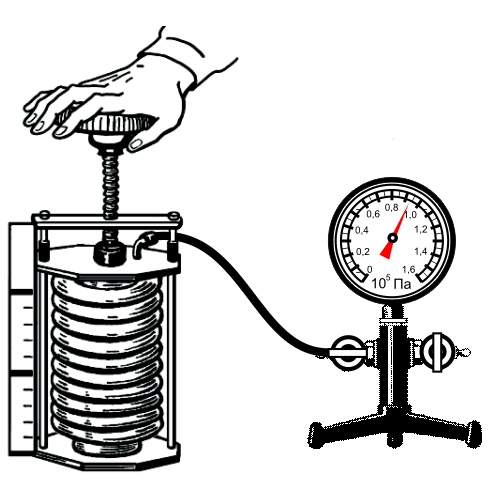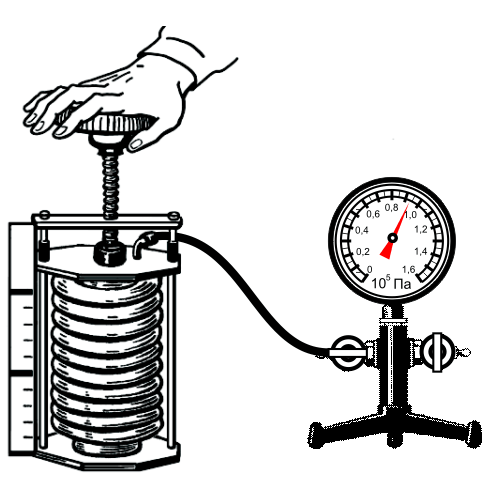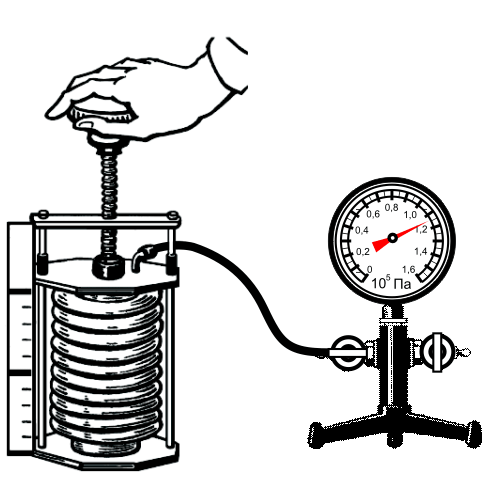
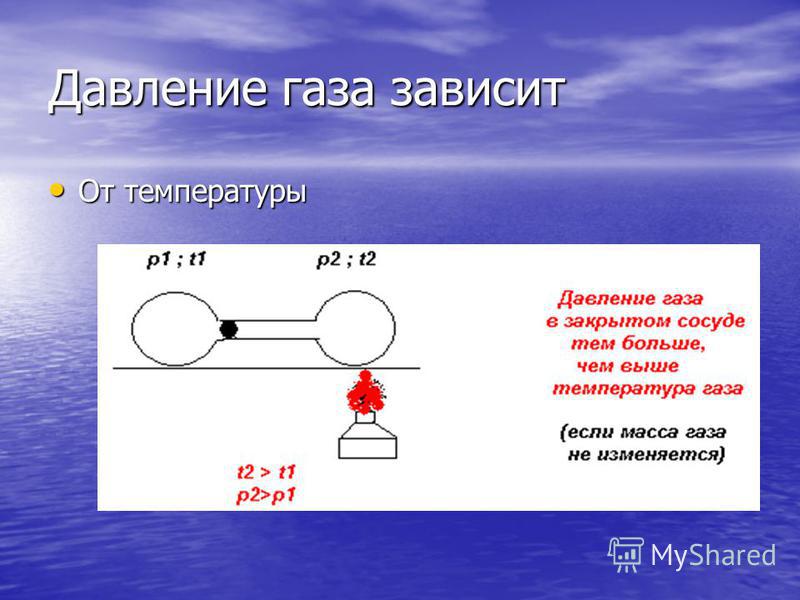


Уравнение Клапейрона-Менделеева достаточно хорошо описывает газ при высоких температурах и низких давлениях, когда он находится в условиях достаточно далёких от условий конденсации. Однако для реального газа это не всегда выполняется и тогда приходится учитывать потенциальную энергию взаимодействия молекул газа между собой. Простейшим уравнением состояния, описывающим неидеальный газ, является уравнение, предложенное в г. Иоханнесом Дедериком Ван-дер-Ваальсом - :. Для различных газов они различны, и их можно определить экспериментально.
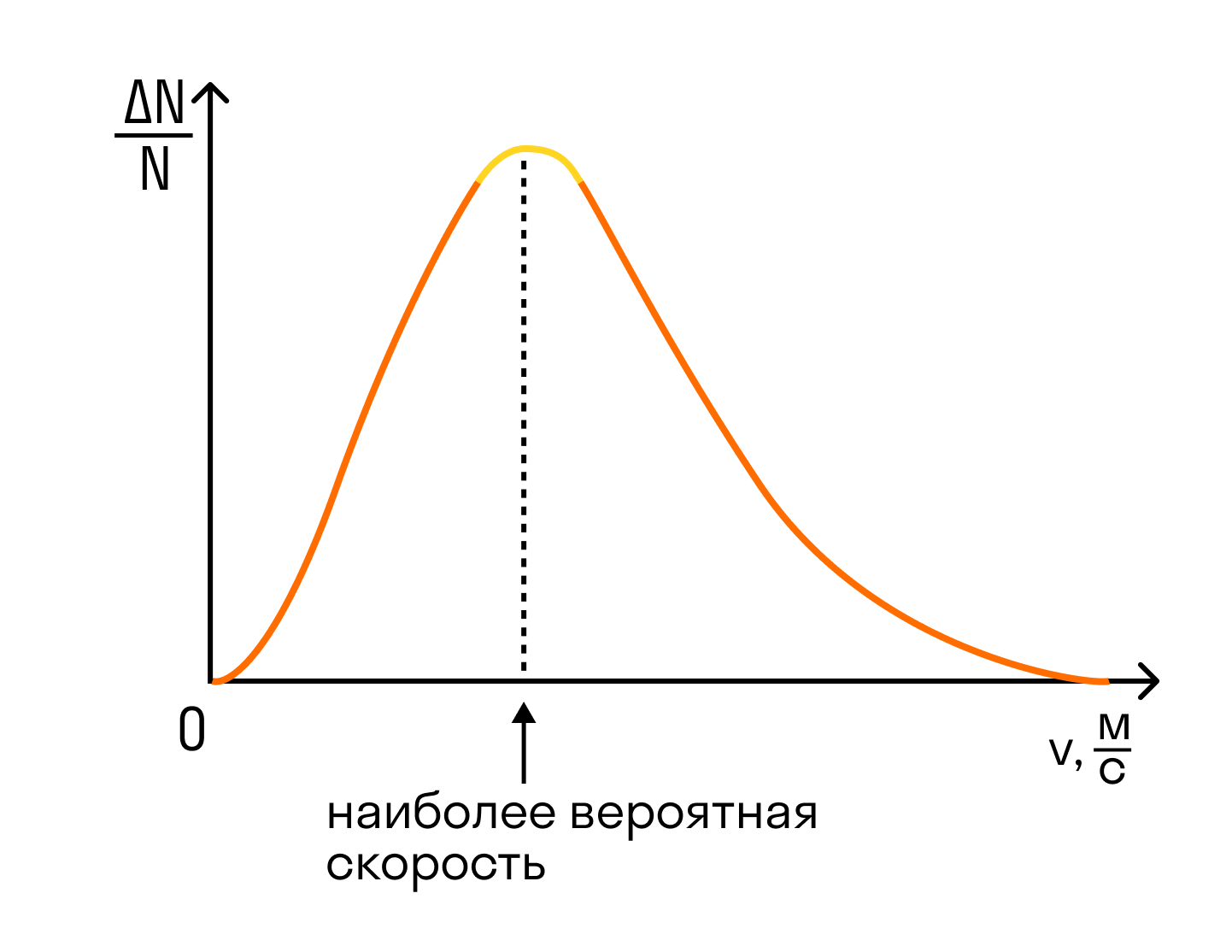


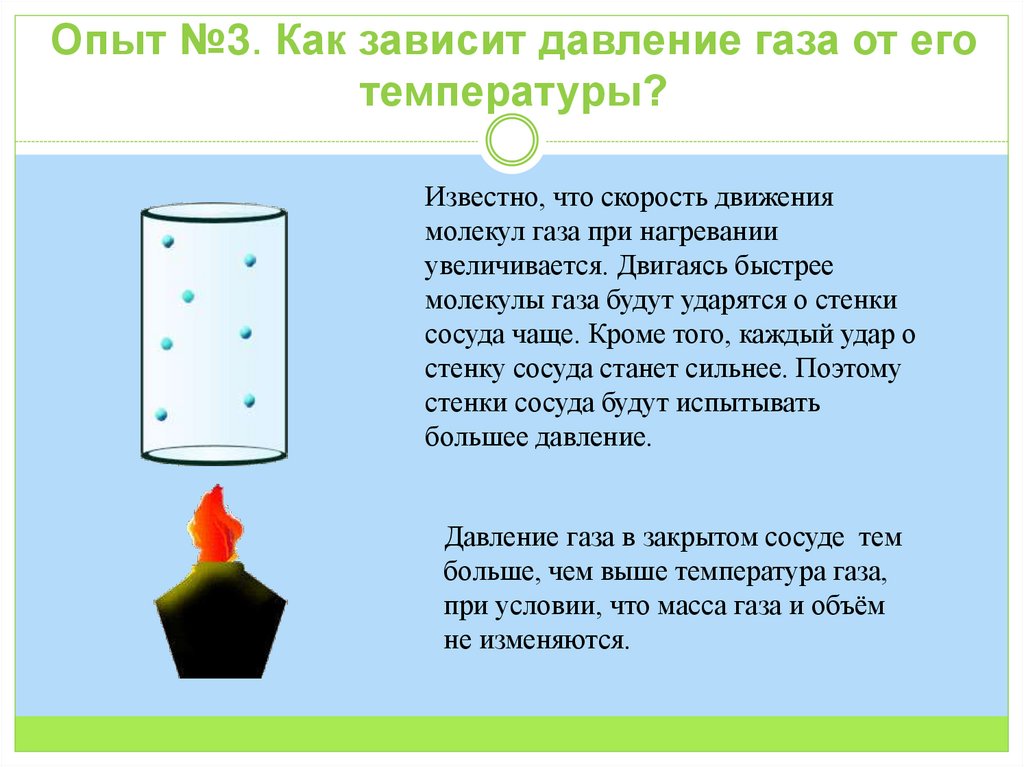



Похожие статьи
- Дизайн спортивный магазин - Дизайн спортивного магазина в ТРЦ Хан Шатыр - antonovich
- Изготовить автоклав своими руками из газового баллона - Автоклав на рыбалке Блог Отшельника
- Купить женскую дубленку модную - Женские дубленки, купить недорого в интернет-магазине в
- Мастер класс открытки учителю своими руками - Инструмент для газоблока: электрический, ручной